Continuamos con la serie de [Química Orgánica]. Por fin dejamos los hidrocarburos atrás y empezaremos a conocer elementos nuevos (bueno, en realidad ya empezamos en el capítulo anterior, con los Halógenos). En este artículo, de hecho, sólo conoceremos al Oxígeno, y en el siguiente al Nitrógeno. Ahí tengo pensado terminar la serie, así que nos quedan, con suerte, dos artículos antes de terminar. Tengo pensado también dedicar un artículo solamente a hacer algunos ejercicios y luego, quién sabe, a lo mejor empiezo con algo de isomería.
Pues bien, aclarado esto, vamos a corregir los compuestos del artículo pasado:
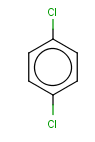
Este compuesto tenía algo de trampa, no mucho, la verdad, supongo que la respuesta intuitiva era 1,4-Diclorobenceno y, aunque el nombre es correcto, hay otro aún más correcto. Teníais que recordar donde hablamos de Xilenos: ahí dijimos que cuando el Benceno tiene dos radicales (y especificamos que si eran Metilos se llamaba Xileno) se podían substituir los localizadores por un prefijo. En concreto, los localizadores 1,4 eran los para-. Así que, la mejor forma de nombrar este compuesto es p-Diclorobenceno.
Luego os pedí que me formularais vosotros unos compuestos que yo os propuse. Vamos a ver cómo tendrían que quedar (no hace falta que sean exactamente iguales, pero sí equivalentes):
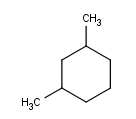
1,3-Dimetilciclohexano (o lo que era lo mismo, m-Dimetilciclohexano)
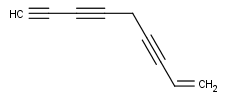
1,3,5-Heptantriino
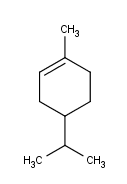
4-Isopropil-1-metilciclohexeno
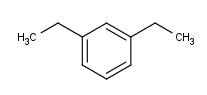
m-Dietilbenceno
1-Nonen-3,6,8-triino
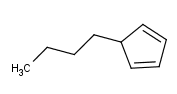
5-Butil-1,3-ciclopentandieno
Y estos eran todos. Como dije en el último artículo, cualquier duda que tengáis ponedla en los comentarios y yo intentaré resolverla lo antes posible.
Ahora sí, vamos a empezar con el Oxígeno y los Compuestos Oxigenados (grupos funcionales). Primero vamos a hacer una tabla/índice de lo que nos toca. Inicialmente los Compuestos Oxigenados iban a ir en un solo artículo, pero como iba a resultar muy largo y denso, he creído conveniente dividir el artículo en dos, igualmente densos, pero más cortos:
- Primera parte:
- Alcoholes
- Aldehídos
- Cetonas
- Segunda parte:
- Éteres
- Ácidos (carboxílicos)
- Ésteres
Vamos allá, empecemos por el principio y expliquemos los Alcoholes:
Alcoholes
Primero de todo vamos a ir dando una clasificación a los compuestos que vayamos explicando. ¿Para qué sirve la clasificación? Es la misma que ya empecé en el artículo anterior, clasificación que ordena los grupos funcionales por orden de prioridad a la hora de nombrar compuestos. Igual que antes los dobles enlaces tenían prioridad ante los radicales, ahora cada uno de los grupos funcionales (no sólo del Oxígeno, sino también del Nitrógeno) tendrá un puesto concreto en el orden de prioridad, que debemos tener clarísimo a la hora de nombrar el compuesto. Bien, por ahora, como solamente hemos hablado de Alcoholes, sólo debéis saber que los grupos funcionales de Alcoholes tienen prioridad ante todo lo que hemos visto hasta ahora (hemos visto que los Alquenos y Alquinos tienen prioridad sobre los Halógenos, que tienen prioridad ante las ramificaciones y que tienen prioridad ante los Alcanos).
Bien, los Alcoholes son un grupo funcional formados por Oxígeno e Hidrógeno (concretamente hidróxido, por si te suena). Vamos a ver por qué se forman:
Si recordamos lo que dijimos en el artículo anterior del porqué de los Halógenos, vamos a ver clarísimo por qué los Alcoholes son como son. Recordemos (aunque seguro que todos lo tenéis perfectamente claro) que los hidrocarburos están formados por Carbonos e Hidrógenos, estando los Carbonos unidos entre ellos y compartiendo los electrones de valencia que les sobran con los Hidrógenos. Bien, pues todos los grupos funcionales del Oxígeno se basan en lo mismo, y es que un Carbono (o más…), en lugar de compartir uno de sus electrones de valencia con un Hidrógeno lo comparte con un Oxígeno. Luego, dependiendo de cómo sea ese enlace se darán diferentes grupos funcionales.
Nuestro caso actual (el del Alcohol) se basa en una unión con un enlace simple entre un Carbono y un Oxígeno; el Oxígeno, por su parte, tiene 6 electrones de valencia,[1] así que, con un electrón ocupado en el enlace con el Carbono, le quedan 5 electrones “libres”. ¿Con qué se unen esos electrones? Podríais pensar que se unen con 5 Hidrógenos, pero no. Por razones que tienen más que ver con la química inorgánica que con la orgánica (ya que se trata de Oxígeno, no de Carbono), el Oxígeno sólo se une a un Hidrógeno (es decir, que usa uno de los electrones para unirse con el Hidrógeno y los otros 4 quedan sin aparear).[2]
Por lo tanto, ya deberíamos tener claro que el Alcohol estará en el lugar donde debería estar un Hidrógeno, sólo que en lugar de H se escribirá OH. Vamos a ver ejemplos claros; si el Metano (CH4) se transforma en un Alcohol pasa a ser (CH3OH). Igual con el Etano (H3C-CH3) que puede convertirse en Alcohol (H3C-CH2OH), por ejemplo.
Esto suele escribirse como R1-OH (la R indica que ahí puede haber cualquier cadena).
Lo último que nos queda saber de los Alcoholes es cómo se nombran porque, evidentemente, el metano no puede llamarse igual que su Alcohol. Pues bien, la nomenclatura es muy fácil: solo se debe añadir el sufijo –ol. Así el Metanol es el alcohol del Metano, el Etanol es el alcohol del Etano, etc.
Pero, como siempre cuando añadimos más Carbonos y hacemos cadenas más largas, necesitamos más información: ¿Dónde está el Alcohol? ¿Cuántos Alcoholes hay? Bien, para dar esas informaciones, igual que con las otras cosas que hemos visto, sólo necesitamos los localizadores, que funcionan igual que siempre, con prioridad en los Alcoholes, y recordad que, si hay más de uno, aparte de los localizadores correspondientes, es importante poner el prefijo correspondiente.
Aparte de esta nomenclatura hay otra nomenclatura alternativa, que incluye la palabra Alcohol y el nombre del radical al cual va unido el grupo funcional. Solo se usa con los radicales simples y con compuestos con un único grupo Alcohol. La nomenclatura es Alcohol de Alquilo (igual que la nomenclatura alternativa que vimos para los compuestos halogenados) y se basa en, primero, escribir la palabra Alcohol y luego el Alquilo al que va unido más el sufijo -ico. Así explicado probablemente no entendáis nada, así que vamos a ver ejemplos. Empezaremos con uno muy famoso:
CH3-CH2OH
Éste compuesto, que antes he nombrado como Etanol, se puede nombrar también como Alcohol etílico (porque el Alcohol va unido al radical Etilo). Seguro que os suena mucho.
Antes de hacer más ejemplos, voy a daros un dato bastante inútil, por ahora:
Cuando haya un Alcohol, pero éste no sea el grupo funcional prioritario (y, por ahora, no hemos visto ninguno que sea más importante que el Alcohol), ya no debe nombrarse con el sufijo –ol, sino que se debe usar un prefijo, concretamente el (Hidroxi-); lo veremos más tarde, pero prefiero adelantarme y decirlo aquí para que lo recordéis luego.
Ahora sí, vamos a ver algunos ejemplos:
Éste es muy fácil. Tenemos una molécula de butano, pero en el Carbono 2 (porque debemos nombrar de derecha a izquierda para que el Alcohol tenga el localizador más bajo) tenemos un Alcohol, por lo tanto, lo nombraremos como 2-Butanol.
Este también es fácil, sólo que el dibujo puede llevar a confusiones: aquí tenemos una molécula de propano con un Alcohol en el Carbono 1. Así que será 1-Propanol.
Éste también es fácil (luego en los deberes ya os lo complicaré un poco más). Éste se trata de una molécula de propano, con un radical Metilo y un Alcohol, ambos en el Carbono 2. Así que, siguiendo el orden que ya sabemos, escribimos que es un 2-Metil-2-propanol.
Información gratuita: Este mismo compuesto se puede nombrar, usando la nomenclatura alternativa como Alcohol tercbutílico (hasta ahora hemos visto el radical isopropil, pero no el tercbutilo, que ya caerá más adelante en la serie).
Pero sigamos con los ejemplos:
¿Aquí ya se complica un poco verdad? Bueno, de hecho tampoco mucho, pues se trata de una molécula de 5 Carbonos, por lo tanto pent-. Tenemos que empezar a numerar para que el Alcohol nos quede en el Carbono 2, así que el doble enlace nos quedará en el Carbono 3 y para nombrar debemos hacer lo siguiente:
Como antes, escribir dónde se encuentra el doble enlace y escribir la molécula:
[3-penten]
Luego decir dónde está el Alcohol y poner el sufijo, pero como no hace falta repetir que es un penteno, sólo pondremos –ol (Algo parecido a lo que hacíamos con los triples enlaces cuando había dobles y triples juntos).
Por lo tanto nos queda un 3-Penten-2-ol.
Aunque puede que ya estéis cansados del Alcohol y queráis pasar a otros grupos, como los Aldehídos, quiero que aburráis tanto el Alcohol que seguiremos con algunos ejemplos más:
Empecemos ya con los nombres largos y complicados característicos de esta serie.
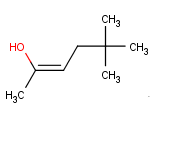
La cadena principal es cualquiera de las tres de 6 Carbonos, y la numeración tiene que hacer que el Alcohol esté en el Carbono 2.
Luego los radicales serán 2 Metilos en el Carbono 5 (independientemente de la cadena elegida), por lo tanto [5,5-dimetil], el doble enlace está en el Carbono 2, así que [5,5-dimetil-2-hexen], y finalmente tenemos un Alcohol en el Carbono 2:
5,5-Dimetil-2-hexen-2-ol
Vamos a seguir practicando, pero entremos en las moléculas cíclicas. No tienen secreto alguno si se ha seguido la serie desde el principio y se han entendido los compuestos cíclicos.
Además, aquí ya tenemos algo que nos llama la atención ¿verdad? Sí, tenemos dos grupos Alcohol en una sola molécula, ¿cómo nombrar esto? Pues igual que cuando tenemos dos radicales o dos dobles enlaces, con un prefijo (ya lo he dicho antes, pero lo repito porque es algo muy importante).
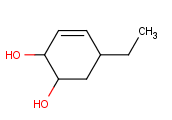
Pero, antes de fijarnos en los Alcoholes, debemos fijarnos en el radical. Si numeramos bien la cadena principal debería saliros que nuestro radical es un [5-etil]; la cadena principal, como tiene un doble enlace en el Carbono 3, es [5-etil-3-ciclohexen], y como tenemos dos Alcoholes en los Carbonos 1 y 2; nuestra molécula se llamará 5-Etil-3-ciclohexen-1,2-diol.
Bien, antes de dejar los Alcoholes tengo que enseñaros algo más, los aromáticos; como vimos en el artículo anterior, suelen tener nombres diferentes, así que vamos a ver como nombraríamos este compuesto:
Os dejo que lo penséis vosotros:
…
…
…
…
…
…
…
…
…
…
Bien, si tu respuesta ha sido Fenol, deja de leer esto y vete a estudiar física cuántica, porqué aquí no vas a aprender nada. Si tu respuesta ha sido Bencenol debo decirte que estás aprendiendo los conceptos a la perfección. Si has llegado a otro nombre, relee algunos conceptos de éste y el artículo anterior. Si no lo has hecho… bueno, tus motivos tendrás.[3]
Bien, este compuesto, en realidad se llama Fenol (aunque el nombre de Bencenol también se acepta, por razones que veremos inmediatamente, pero nadie lo usa), como todos los aromáticos es cuestión de recordar este nombre para poder nombrar compuestos como éste:
Que, con 3 radicales Metilo se llamaría 3,4,5-Trimetilfenol (recordemos que se empieza a numerar desde el Alcohol y, en este caso, da igual el sentido que escojas).
Y vamos a ver por qué también se acepta el nombre de Bencenol en lugar de Fenol:
Este compuesto es aromático, pero como no se le puede llamar ni Difenol ni Fendiol ni nada parecido, sigue la nomenclatura tradicional (sí, los aromáticos suelen dar dolor de cabeza a más de uno…). Así que este compuesto, al ser un Benceno como cadena principal y tener dos Alcoholes en los Carbonos 1 y 2, se llama 1,2-Bencendiol, pero… ¿se podría formular de otra manera? Sí, y de hecho la forma más correcta de hacerlo es ésta: o-Bencendiol. (Si no ves el porqué del nombre, vuelve a leer el artículo anterior).
Y finalmente, antes de terminar con los Alcoholes, vamos a ver un compuesto que quizás tengas ahora mismo en tu casa:
Se trata del 1,2,3-Propantriol, más conocido como glicerol o glicerina.
Bien, ahora sí, después de un largo rato con los Alcoholes, vamos a seguir con el siguiente grupo funcional.
Aldehídos
Los Aldehídos son otro grupo funcional de los compuestos oxigenados. Es un grupo funcional con más importancia –prioridad- que los Alcoholes, así que vamos a actualizar nuestra clasificación para que todos la tengáis muy clara:
Aldehídos → Alcoholes → Alquenos y Alquinos → Compuestos Halogenados → Radicales → Alcanos.
Bien, ¿recordáis lo que dijimos antes, al hablar del porqué de los Alcoholes? Dijimos que el Oxígeno se unía mediante un enlace simple con un Carbono y con otro enlace simple con un Hidrógeno (y que, por razones inorgánicas, sólo dos de sus 6 electrones se unían a otro átomo). Pues los Aldehídos son algo distinto. En este caso, igual que antes, sólo dos electrones del Oxígeno se unen a otro átomo, pero esta vez los dos electrones del Oxígeno se unen al mismo Carbono (es decir, que el Oxígeno se une al Carbono con un enlace doble). Pero esto no es todo, ya que aparte de los Aldehídos podrían haber otros grupos funcionales que se unan al Carbono con un doble enlace (y si digo esto, ya deberías suponer que sí los hay). Para que el grupo funcional sea un Aldehído es importantísimo que el Carbono al que está unido el Oxígeno esté unido con otro Carbono mediante un enlace simple y con un Hidrógeno. Esto que acabo de decir suele simplificarse diciendo que el Carbono al que se une el Oxígeno debe estar en un extremo. Lo que no me gusta de esta definición es que no es válida para todos los casos. Y, aunque todos los Aldehídos cumplan esta “norma”, no todos los compuestos que cumplen esta norma son Aldehídos. Por lo que, dado que esta norma sirve para identificar Aldehídos… pues no le veo la gracia (ya veremos un ejemplo de esto al hablar de otro grupo).[4]
Vamos a ver cómo se formula normalmente un Aldehído:
Como veis, el Carbono solo puede unirse a la cadena (R1) pero no puede continuarla, ya que debe unirse a un átomo de Hidrógeno. Por eso funciona la norma de que todos los Aldehídos están en un extremo de la cadena (que, como he dicho, no es recíproca).
Vamos a ver un ejemplo para saber cómo nombrar los Aldehídos:
Bien, la cadena principal tiene que ser la que incluye el Aldehído y el doble enlace, ésta tiene 5 Carbonos (si no la ves, es la que empieza por el Carbono del Aldehído y termina en el H3C de abajo a la izquierda).
Si numeramos siguiendo el orden que he dicho antes (es decir, empezando por el Aldehído), vemos que tenemos radicales Metilo en los Carbonos 2 y 3 (que no os confunda ese hidrógeno suelto, eso no es un radical, forma parte del Aldehído) y luego vemos un doble enlace (tampoco debéis confundiros con el doble enlace del Oxígeno, que también forma parte del Aldehído) en el Carbono 3. Luego, como casi todos los grupos funcionales se nombran en forma de sufijo, podemos deducir que el compuesto será [2,3-dimetil-3-penten…]
Y simplemente tendremos que añadir el sufijo de los Aldehídos; que es –al.
Por lo tanto esa molécula es 2,3-Dimetil-3-pentenal.
Fijaos que no se pone el localizador del Aldehído; eso es porque, por lo que sabemos hasta ahora, el Aldehído siempre estará en el Carbono 1, y por lo tanto no es necesario indicarlo.
NOTA: No siempre el Aldehído estará en el Carbono 1, pero ya os avanzo que no se tiene que poner prefijo, ya que siempre sabremos si está en el Carbono 1 o en otro. Pero por otra parte sí es importantísimo (y aquí mucho más que en cualquier otro visto antes) poner el prefijo si hay más de un Aldehído. Vamos a ver un ejemplo:
Aquí vemos claramente cómo hay dos Aldehídos, uno en cada extremo de la cadena. Nombrar este compuesto no debería resultar difícil si se han entendido los conceptos (de este artículo y anteriores) adecuadamente.
La cadena principal es de 5 Carbonos, y hay dos radicales Metilo en los Carbonos 2,3. Así que nuestra molécula es
2,3-Dimetilpentandial
Como vemos, no se indica dónde están los Aldehídos, pero sí que hay dos (los dos últimos compuestos que acabamos de hacer son prácticamente iguales y, aparte del doble enlace, si no indicáramos el prefijo vemos que puede llevar a confusiones).
Antes de terminar, ya sabéis que siempre se busca simplificar al máximo la formulación de los compuestos, por lo que, en lugar de hacer todo ese dibujito que he hecho yo, es muy común ver los Aldehídos como (-CHO) o (OHC-).[5]
Luego… hay otra nomenclatura de la que os quiero hablar. Es posible formular los Aldehídos usando el sufijo –carbaldehído en lugar del sufijo –al. Esta forma de nombrar no la veréis nunca en compuestos de cadena abierta (si no recordáis qué son los compuestos de cadena abierta echad un vistazo a este artículo), sólo en compuestos cíclicos, que es donde se suele utilizar. Aun así, a veces se lee por ahí que, si un Aldehído es cíclico se debe utilizar esta nomenclatura, siendo la otra errónea. Esto no es así, y ambas son correctas (de hecho, yo solo usaré el sufijo –al).
Y finalmente, igual que hicimos con el grupo Alcohol, voy a daros una información que no nos servirá por ahora, pero debemos tener presente para cuando nos aparezcan varios grupos en un mismo compuesto. Si el Aldehído NO es el grupo funcional prioritario, en lugar de escribir el sufijo –al, se usa el prefijo formil-.
Cetonas
Las Cetonas son otro grupo funcional de los compuestos oxigenados (si no, ¿para qué iba yo a hablar de ellas aquí?). Su orden de prioridad está entre los Aldehídos y los Alcoholes, por lo que, actualizando nuestra lista, nos queda algo así:
Aldehídos → Cetonas → Alcoholes → Alquenos y Alquinos → Compuestos Halogenados → Radicales → Alcanos.
Como hasta ahora, vamos a ver qué hace especial a las Cetonas:
Las Cetonas son muy parecidas a los Aldehídos (y en muchas ocasiones suelen enseñarse juntos), pero vamos a ver qué tienen de parecido y qué los diferencia. En las Cetonas, igual que en los Aldehídos, el Oxígeno se une al Carbono mediante un doble enlace, pero, esta vez, a diferencia de los Aldehídos, el Carbono al que va unido el Oxígeno no tiene que estar unido a un Hidrógeno. Esto permite que la Cetona esté en medio de una cadena, en lugar de estar siempre en un extremo (como pasa con los Aldehidos). E, igual que en todos los casos vistos hasta ahora, el Oxígeno sólo comparte dos electrones, por lo que, al usarlos con el mismo Carbono, impide que el oxígeno se una a nada más.
Vamos a ver la forma general de una Cetona
Podemos ver que hay un Oxígeno unido a un Carbono con un doble enlace y que este Carbono se une a dos cadenas (lo que forma una sola cadena). Y una vez enseñada la forma general, vamos a mostrar algunos ejemplos para aprender a nombrarlas
Aquí tenemos a un hexano con una Cetona en el Carbono 3 (ya que, si recordamos el orden de prioridad, sabemos que la Cetona es más importante que los Alcanos, y debemos dejarla en el mínimo localizador posible). Por lo tanto, si yo os digo que el sufijo que se usa para las Cetonas cuando son el grupo funcional prioritario es (–ona), no debería ser difícil nombrar este compuesto ¿verdad?
Bien, efectivamente es un 3-Hexanona
Vamos a ver más casos:
Este puede que parezca un poco más difícil, pero creo que debería ser igual de sencillo que el anterior. Tenemos la cadena principal muy clara. Luego, dado que la mejor numeración es la que tiene las Cetonas en los Carbonos 1 y 3 y el Metilo en el Carbono 4, nuestra molécula se llamará 4-Metil-1,3-ciclopentandiona.
Bien, recordaréis que antes, al hablar de los Aldehídos, dije que a mí me enseñaron una norma que no siempre se cumplía. Básicamente, dado que los Aldehídos y las Cetonas son los dos únicos grupos funcionales en los que el Oxígeno va unido al Carbono mediante un enlace doble (bueno, esto es una mentida como una catedral, pero no nos adelantemos a los sucesos), suele oírse por ahí que “Si el grupo funcional se encuentra en un extremo de la cadena, se trata de un Aldehído; si, por lo contrario, se encuentra en medio, es una Cetona”.
Entonces vamos a formular éste compuesto. Lo primero de todo es decidir una cosa primordial. ¿Se trata de un Aldehído?, ¿O se trata de una Cetona? Siguiendo la norma que acabo de decir sería un Aldehído, ya que se encuentra en uno de los extremos de la cadena. Pero si recordamos las “normas” que yo dije al hablar de ellos nos daremos cuenta de que no puede serlo, ¿Por qué? ¡Pues porque el Carbono al que está unido el Oxígeno no está unido a ningún Hidrógeno! Por lo tanto, podemos afirmar que, aunque esté en el extremo de una cadena, el grupo funcional de la molécula anterior es una Cetona.
Formular el compuesto una vez sabemos que es una Cetona no es tan complicado. Primero de todo identificamos un radical Metilo en el Carbono 3, luego vemos que en el Carbono 1 hay un doble enlace, y que en el mismo Carbono 1 está la Cetona. Finalmente contamos los Carbonos de la cadena y vemos que se trata de una cadena de 5 Carbonos. Por lo tanto el compuesto es
3-Metil-1-penten-1-ona
Igual que siempre, las Cetonas no tienen por qué ser el grupo funcional prioritario (los Aldehídos tienen más prioridad, por ejemplo), por lo tanto, debemos saber que si nos aparece un grupo Cetona sin ser el prioritario, debemos nombrarlo con el prefijo oxo-.
También, igual que los Aldehídos (-CHO o OHC-) y los Alcoholes (-COH-) las cetonas pueden escribirse de una forma mucho más cómoda como (-CO- o -OC-[6]).
Antes de terminar, las Cetonas también tienen una nomenclatura alternativa. La nomenclatura se basa en considerar el Carbono al que está unida la Cetona como único Carbono de la cadena principal, y las otras cadenas a las que se une, considerarlas como radicales. Así la nomenclatura que se usa es
|
Radical 1 |
+ |
Radical 2 |
+ |
Cetona |
Así, éste compuesto[7] se puede nombrar como 1-Fenil-1-propanona o, siguiendo la nueva nomenclatura, como Etil fenil cetona.
Hemos hablado sobre Alcoholes, Aldehídos y Cetonas en esta primera parte, podríamos practicar algo más con la nomenclatura alternativa de las Cetonas, pero hay un grupo que se nombra casi igual, los Éteres. Pero hablando de los Éteres…
- la configuración del Oxígeno es 1s2 2s2 2p4 [↩]
- De hecho, las razones son simples, y si recordáis la introducción deberíais poder deducirlo [↩]
- Parezco una de esas maquinillas telefónicas: “Si quiere hablar con Pepito, pulse 1; si quiere hablar con María, pulse 2; si desea hablar con Juan, pulse 3.” [↩]
- A mí me enseñaron la definición que no me gusta, y tuve que pelearme con esos compuestos que no la cumplen, así que yo mismo me inventé esta otra, que en principio debería funcionar siempre… aunque no estoy seguro. [↩]
- OJO: Antes de usar esas abreviaturas es importante dominar un poco el tema, ya que no es lo mismo CHO (Aldehído) que COH (Alcohol). [↩]
- siempre se usa la primera, de hecho, -OC- nunca lo he visto escrito ni lo he escrito yo nunca, así que ni siquiera sé si es correcto… [↩]
- que, por cierto, es otro de los que no cumple con la regla de “todo lo que está en un extremo es un Aldehído” [↩]

The [Química Orgánica] IV-Compuestos Oxigenados (I) by Roger Balsach, unless otherwise expressly stated, is licensed under a Creative Commons Attribution-Noncommercial-No Derivative Works 2.5 Spain License.


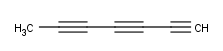


















{ 1 } Comentarios
En la vida cotidiana van a encontrarse que la gente llama a algunos de estos compuestos con otros nombres:
Acetaldehido = Etanal Formol = Formaldehido = Metanal
Si te estas preguntando ¿Por que demonios le dicen formol a un aldehido en lugar de a un alcohol?. Pues, yo tampoco tengo idea.
Lo mismo sucede con el toluol, otro nombre que usa la gente para el tolueno (Que de alcohol no tiene nada).
PD: informo una pequeña errata: “mentida” en lugar de “mentira”.
Escribe un comentario